jeun
admin


 |  Sujet: Le sens 'spontané' d'évolution d'un système est-il prévisible? Sujet: Le sens 'spontané' d'évolution d'un système est-il prévisible?  3/11/2012, 17:49 3/11/2012, 17:49 | |
|
Le sens d'évolution d'un système chimique peut-il être inversé ?
- Un système chimique évolue spontanément vers l'état d'équilibre
- Quotient de réaction,  : expression littérale (rappel) et calcul de sa valeur pour un état quelconque donné d'un système. : expression littérale (rappel) et calcul de sa valeur pour un état quelconque donné d'un système.
- Au cours du temps, la valeur du quotient de réaction  tend vers la constante d'équilibre (critère d'évolution spontanée). tend vers la constante d'équilibre (critère d'évolution spontanée).
- Illustration de ce critère sur des réactions acido-basiques et des réactions d'oxydoréduction.
- Les piles, dispositifs mettant en jeu des transformations spontanées permettant de récupérer de l'énergie
-
Transferts spontanés d'électrons entre des espèces chimiques (mélangées
ou séparées) de deux couples oxydant/réducteur du type ion
métallique/métal, 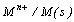 . .
-
Constitution et fonctionnement d'une pile : observation du sens de
circulation du courant électrique, mouvement des porteurs de charges,
rôle du pont salin, réactions aux électrodes. La pile, système hors
équilibre au cours de son fonctionnement en générateur.
Lors de
l'évolution spontanée, la valeur du quotient de réaction tend vers la
constante d'équilibre. La pile à l'équilibre "pile usée" : quantité
d'électricité maximale débitée dans un circuit.
- Force électromotrice d'une pile (f.é.m.) E : mesure, polarité des électrodes, sens de circulation du courant (en lien avec le cours de physique).
- Exemple de pile usuelle.
- Exemples de transformations forcées- Mise en
évidence expérimentale de la possibilité, dans certains cas, de changer
le sens d'évolution d'un système en imposant un courant de sens inverse à
celui observé lorsque le système évolue spontanément (transformation
forcée).
- Réactions aux électrodes, anode et cathode.
- Application à l'électrolyse : principe et exemples d'applications courantes et industrielles.
| |
|
